Le principal élément des dispositifs CurieuzenAir fixés aux fenêtres, ce sont leurs « narines ». Il s’agit bien sûr des tubes gradués, connus sous le nom de tubes de Palmes. Mais de quoi s’agit-il précisément ? Et comment fonctionnent ces tubes ? Si le résumé dans l’illustration – cliquez sur l’image pour l’agrandir – ne suffit pas, vous trouverez ci-dessous une explication plus détaillée, mais aussi un peu plus aride, pour les personnes qui possèdent quelques connaissances techniques et scientifiques.
Comment fonctionnent les tubes de mesure ?
L’explication scientifique complète, pour les participants intéressés ou pour aborder le sujet avec ses élèves
Principe des tubes gradués et de l’analyse chimique
Le tube se compose d’un corps en acrylique, d’un bouchon jaune et d’un bouchon noir. Si vous regardez bien, vous verrez que le bouchon noir contient un petit morceau de gaze métallique. En fait, il y a même deux morceaux de gaze l’un derrière l’autre. Ils servent de support à la substance qui nous permet de réaliser les mesures, la triéthanolamine, TEA en abrégé, ajoutée à un gel aqueux. Tout au long de la période de mesure, la TEA transforme le dioxyde d’azote (NO2) en nitrite, qui se fixe dans le gel. Les laborantins veillent donc à tenir les tubes éloignés de toute source de NO2 le temps des préparatifs, jusqu’à leur fermeture par le bouchon jaune.
Une fois qu’ils sont placés dans le panneau et que le bouchon jaune est ôté, le NO2 se concentre sur les morceaux de gaze. La réaction chimique qui se fait entre le NO2 et la triéthanolamine contenue dans le gel dont est imprégnée la gaze produit du nitrite qui est fixé par le gel. Le mécanisme suivant est proposé pour cette réaction :
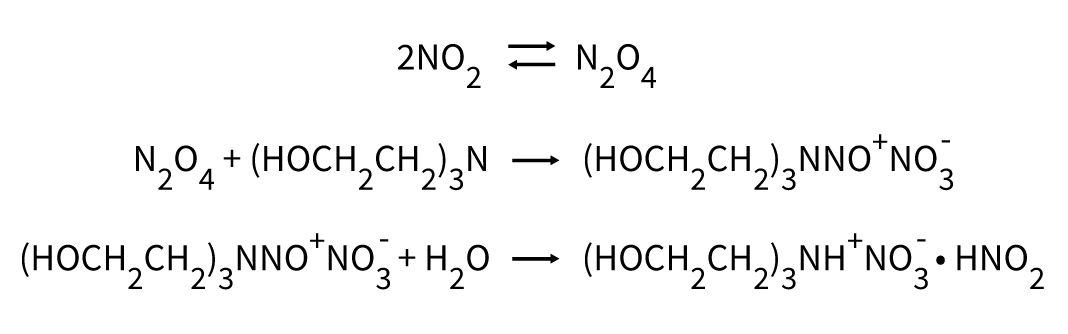
Du fait de cette réaction, la concentration atmosphérique de NO2 est égale à 0 au niveau de la gaze, si bien qu’il y a une diffusion nette de NO2 provenant de l’extérieur du tube jusqu’aux morceaux de gaze. Cette diffusion est régie par des lois physiques (première loi de diffusion de Fick), tandis que sa rapidité dépend de la température, des dimensions du tube et de la concentration de NO2 dans l’air. La quantité de nitrite sur la gaze nous permet donc de calculer la concentration moyenne en NO2 dans l’air sur le site de mesure pendant la période de mesure.
Au terme de cette période, le tube retourne au laboratoire. Celui-ci calcule la quantité de nitrite qui s’est accumulée sur la gaze, ce qui nous permet de calculer la concentration moyenne de NO2. La gaze est rincée à l’eau qui récupère le nitrite. Du réactif de Saltzman-Griess, un mélange de substances chimiques, est ensuite ajouté à l’eau et transforme le nitrite en un colorant violet (N-alpha-naphthyl-éthylènediamine).
Un spectrophotomètre contrôle la concentration de nitrite dans l’eau en mesurant le degré d’absorption d’une longueur d’onde correspondant à la couleur violette. La concentration de nitrite dans cette eau peut ensuite être multipliée par le volume de celle-ci afin d’obtenir la quantité totale de nitrite fixé sur les morceaux de gaze. Nous pouvons donc calculer la concentration moyenne en NO2 au moyen de la formule suivante :
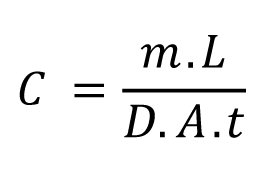
Dans cette formule, m correspond à la masse calculée du nitrite présent sur la gaze, L est la distance qui sépare l’ouverture du tube des morceaux de gaze, D le coefficient de diffusion du NO2 dans l’air, A la section transversale du tube et t la période de mesure, c’est-à-dire la durée pendant laquelle le tube est resté ouvert. La valeur D est donnée par la littérature scientifique pour des conditions normales de pression et de température, puis corrigée en fonction de la température et de la pression moyennes pendant la période de mesure. Les autres grandeurs sont connues.
Partir de concentrations brutes pour obtenir des concentrations représentatives pour la période de mesure
Cette concentration fait l’objet d’une autre correction encore. Il y a deux tubes par site et le résultat moyen de ces deux tubes permet d’obtenir une mesure d’une précision correcte. Il s’agit du degré de correspondance qui serait obtenu entre les résultats de plusieurs mesures dans les mêmes circonstances. Nous savons cependant que le résultat moyen de cette méthode pratique diverge de la valeur réelle, qui est mesurée avec plus de précision par des appareils aussi chers que sophistiqués. La méthode de référence pour la mesure du NO2 se base sur la chimiluminescence.
Pour corriger cet écart, une mesure de calibration s’effectue en parallèle, simultanément sur huit stations de mesure de Bruxelles Environnement et deux du Parlement européen qui utilisent cette méthode de référence. Deux stations de mesures supplémentaires louées à l’Institut Scientifique de Service Public (ISSeP) ont également été installées par nos soins. Nous fixons donc nos panneaux sur ces stations et calculons le rapport entre les résultats que nous obtenons et ceux de la méthode de référence. Ce rapport sert ensuite à corriger les concentrations brutes pour obtenir les résultats définitifs que nous intègrerons dans notre rapport sur les mesures en mars.
Calcul des moyennes annuelles
Mais pour interpréter les résultats, nous devons encore convertir les résultats des mesures obtenus en mars en moyennes annuelles. Cette conversion s’impose avant tout parce que les concentrations en NO2 varient tout au long de l’année, et sont généralement plus élevées en hiver. Les émissions de NO2 évoluent en effet de mois en mois, la météo exerçant un impact non négligeable sur les concentrations en NO2 dans l’air. La pluie par exemple réduit les concentrations en NO2 dans l’atmosphère, ce qui provoque des différences entre les périodes pluvieuses et les périodes plus sèches.
Une autre raison vient du fait que les directives relatives à l’exposition au NO2 de l’Union européenne comme de l’Organisation mondiale de la santé sont formulées sur une base annuelle. Cette moyenne annuelle est donc nécessaire pour effectuer des comparaisons avec ces directives.
Les concentrations définitives sont converties en moyennes annuelles au moyen d’un facteur. Celui-ci tient compte aussi bien des concentrations en NO2 mesurées par les stations de mesure de référence que de la météo des 12 mois écoulés.
Détails supplémentaires
Pourquoi est-il préférable de conserver les tubes au réfrigérateur puisqu’ils prennent de toute façon des mesures en plein air ?
Avant les mesures : la lumière du soleil et la chaleur provoquent la libération de résidus de NO2 contenu dans le tube ou les bouchons, lesquels sont ensuite absorbés par la gaze et viennent fausser les résultats à la hausse.
Après les mesures : la lumière du soleil et la chaleur brisent définitivement la liaison entre la TEA et le NO2, ce qui produit des valeurs inférieures à la réalité.
Des mesures de protection sont intégrées à l’avance dans la méthode de mesure. Pendant la période de mesure, les morceaux de gaze imprégnés de TEA sont orientés de manière que l’ouverture soit tournée vers le bas, ce qui les met à l’abri de la lumière directe du soleil. Ils sont par ailleurs placés dans un bouchon noir, lequel absorbe la lumière indirecte du soleil avant qu’elle puisse les atteindre.
Qu’est-ce qui peut perturber les mesures ? Comment gérez-vous ces facteurs de perturbation ?
Comme nous l’avons dit précédemment, le principe des mesures repose sur la diffusion du dioxyde d’azote régie par la première loi de diffusion de Fick. Les dimensions du tube conditionnent la distance de diffusion et sa rapidité. Des facteurs qui jouent un rôle à ce niveau risquent donc de perturber les mesures. Si le tube est exposé au vent par exemple, celui-ci peut souffler les molécules de dioxyde d’azote dans le tube sur une certaine distance (turbulence), ce qui raccourcit la distance de diffusion. Le dioxyde d’azote pourra donc se lier plus vite et les concentrations dans l’air seront surestimées. Les obstacles qui ralentissent la diffusion, notamment une toile d’araignée, freinent quant à eux la vitesse de diffusion, ce qui va aboutir à une sous-estimation.
L’exposition au vent est gérée au moyen du panneau qui permet de placer les tubes à bonne distance de la façade (une trop grande proximité avec celle-ci les expose aux effets de la turbulence des vents) tout en leur offrant une certaine protection.
Il faut également éviter que de l’humidité pénètre à l’intérieur des tubes, car l’eau emporterait la TEA et le nitrite, c’est d’ailleurs le principe sur lequel se base l’analyse. Ce qui explique que l’ouverture doit être orientée vers le bas. L’humidité atmosphérique n’a qu’une influence limitée et n’est généralement pas prise en compte.
La réaction chimique indique que l’ensemble du dioxyde d’azote n’est pas transformé en nitrite, n’est-ce pas ?
Selon les formules citées plus haut, le rapport nitrite/dioxyde d’azote devrait être de 0,5. Un rapport de 0,6 à 0,7 a été obtenu expérimentalement aux concentrations habituelles dans notre air, qu’elles soient faibles ou élevées. C’est seulement à des concentrations très élevées (sources de combustion dans des espaces clos) que le rapport théorique de 0,5 a été observé. L’écart par rapport à cette valeur pour les concentrations pertinentes s’explique probablement par des réactions parallèles, mais sans certitude. La correction se fait notamment au moyen de la calibration effectuée dans les stations de mesure de référence, car ce problème ne se pose pas pour les mesures de référence basée sur la chimiluminescence.











